
臨床成績
本剤は、承認外の効能又は効果、用法及び用量による臨床試験の成績も含めた臨床データパッケージで評価され承認された。そのため、国内で承認されている効能又は効果、用法及び用量と異なるデータも紹介する。
1.臨床データパッケージ1)
| 試験の種類・ 相試験番号 | 試験国 | 対象・例数 | 試験目的 | 試験デザイン |
|---|---|---|---|---|
| 海外第Ⅰ相 AVT03-GL-P01 試験 (海外データ) | ニュージーランド、オーストラリア、南アフリカ | 健康成人男性 206例 | 本剤60mg#単回皮下投与時の安全性及び忍容性等の評価に加えて、先行バイオ医薬品(US)の60mg製剤*1との薬物動態(PK)の同等性/同質性を検討する | ランダム化、二重盲検、単回投与、2群並行、群間比較試験 |
| 海外第Ⅰ相 AVT03-GL-P03 試験 (海外データ) | 英国、ポーランド、南アフリカ | 健康成人男性 204例 (日本人24例) | 本剤120mg単回皮下投与時の安全性及び忍容性の評価に加えて、先行バイオ医薬品(US)の120mg製剤*2との薬物動態の同等性/同質性を検討する | ランダム化、二重盲検、単回投与、2群並行、群間比較試験 |
| 海外第Ⅲ相 AVT03-GL-C01 試験 (海外データ) | ブルガリア、チェコ、ジョージア、ポーランド、南アフリカ | 50歳以上の閉経 後骨粗鬆症患者 (女性) 532例 | 本剤60mg#と先行バイオ医薬品(US)の60mg製剤*1の有効性の同等性を検討する | ランダム化、二重盲検、反復投与、2群並行、群間比較、多施設共同試験 |
# AVT03-GL-P01試験及びAVT03-GL-C01試験では、国内未承認である本剤の皮下投与用プレフィルドシリンジ(PFS)製剤を用いて実施した。
*1 先行バイオ医薬品(US)の60mg製剤は米国で承認されているプラリア®〔デノスマブ(遺伝子組換え)製剤〕を指す。
*2 先行バイオ医薬品(US)の120mg製剤は米国で承認されているランマーク®〔デノスマブ(遺伝子組換え)製剤〕を指す。
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
本試験には承認外の効能又は効果、用法及び用量の情報が含まれているが、本剤と先行バイオ医薬品(US)の60mg製剤*1との有効性の同等性を検討した承認時評価資料のため紹介する。
2.海外第Ⅲ相臨床試験(AVT03-GL-C01試験)2,3)(海外データ)
2)社内資料:海外第Ⅲ相臨床試験成績(AVT03-GL-C01)[承認時評価資料]
3)Lortkipanidze M, et al.: Expert Opin Biol Ther. 2025; 25(8): 899-912
(COI:本試験はAlvotech社の資金提供により実施された。著者の中にAlvotech社の社員が含まれる)
本剤と先行バイオ医薬品の臨床的同等性を比較するための臨床試験に関して、ランマーク®の有する効能又は効果の対象疾患では、併用薬、疾患の状態や病期などの交絡因子により、治療反応の正確な評価が困難であること、また、以下の1~3の要因により、対象として、デノスマブを有効成分とするプラリア®の効能又は効果である骨粗鬆症のうち、閉経後女性患者が感度の高い集団であると考えられた。
- プラリア®の有する効能又は効果である骨粗鬆症では、男性と比較して、骨粗鬆症の閉経後女性でデノスマブの治療効果がより高かった4,5)。ステロイド性骨粗鬆症では、併用薬、疾患の状態や病期などの交絡因子により、治療反応の正確な評価が困難である。
- 骨粗鬆症を有する閉経後女性における骨密度増加に対するデノスマブの有効性は十分に確立されており、椎骨骨折、非椎骨骨折及び大腿骨近位部骨折のリスクを有意に低下させることが示されている6-8)。
- 閉経後女性の骨粗鬆症の有病率は他の効能又は効果の疾患と比較して高いことから、必要な期間内に適切な患者数を確保できる可能性が高いと考えられた9-11)。
以上から、本剤と先行バイオ医薬品の臨床的同等性を比較するための臨床試験では、骨粗鬆症の閉経後女性患者を対象に、本剤の60mg製剤と米国で承認されているプラリア®の臨床的同等性を比較した。
試験概要
| 目的 | 50歳以上の閉経後骨粗鬆症患者を対象に、本剤の先行バイオ医薬品(US)の60mg製剤*1に対する12ヵ月時点での腰椎骨密度のベースラインからの変化率の同等性について評価する。 | ||||
|---|---|---|---|---|---|
| 試験デザイン | ランダム化、二重盲検、反復投与、2群並行、群間比較、多施設共同試験 | ||||
| 対象 | 50歳以上の閉経後骨粗鬆症患者(女性)532例 | ||||
| 試験方法 | 対象を、閉経からの経過年数及び骨粗鬆症に対する生物学的製剤による治療歴を層別因子として層別し、本剤60mg群(本剤60mgを初回投与し、その後は6及び12ヵ月目に皮下投与)又は先行バイオ医薬品群〔先行バイオ医薬品(US)の60mg製剤を初回投与し、その後は6ヵ月目に皮下投与〕のいずれかに1:1の割合でランダムに割り付けた。先行バイオ医薬品群では同様の層別因子により層別し、先行バイオ医薬品-本剤群(12ヵ月目に本剤60mgを皮下投与)又は先行バイオ医薬品-継続群〔12ヵ月目に先行バイオ医薬品(US)の60mg製剤を皮下投与〕のいずれかに1:1の割合でランダムに割り付けた。 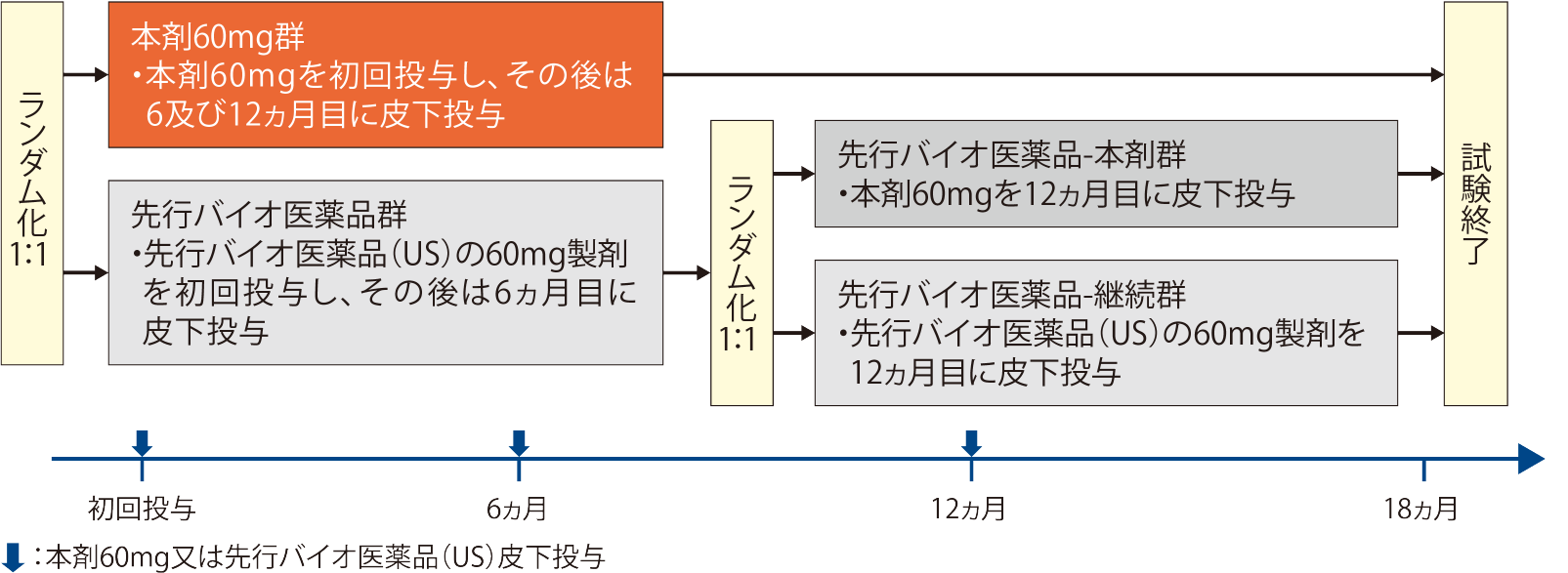 | ||||
| 主要評価項目 | [有効性] 12ヵ月時点での腰椎骨密度のベースラインからの変化率[検証的解析項目] | ||||
| 副次評価項目 | [有効性]
[安全性]
[免疫原性]
[薬物動態(PK)]
[薬力学(PD)]
| ||||
| 解析計画 | [有効性の解析]主要評価項目は、治験薬を1回以上投与したすべての患者を含む最大の解析対象集団(FAS)を対象として解析した。
[安全性の解析] 有害事象*3は、安全性解析対象集団*4を対象として解析し、有害事象の発現患者数及び割合を要約した。 [免疫原性の解析] 安全性解析対象集団で、抗薬物抗体(ADA)及び中和抗体(nAb)の有無を投与群別、治験期間別に集計した。 [PK・PDの解析] PKの解析はPK解析対象集団*5を対象とした。 治療期間別に血液検体を採取し、本剤60mg群及び先行バイオ医薬品群の血清中デノスマブ濃度を評価した。 血清中トラフ濃度は、180日目、12ヵ月目の投与前に採取した検体により解析を実施した。 PDの解析は、PD解析対象集団*6を対象とした。 %Cfb sCTX-1のAUEC0-6monthsの解析は、治療差の過小評価につながる可能性のある中間事象が認められた患者を解析から除外した。 | ||||
| 試験期間 | 2022年8月23日(最初の患者の初回来院)~2024年10月28日(最後の患者の最終来院) |
*1 先行バイオ医薬品(US)の60mg製剤は米国で承認されているプラリア®〔デノスマブ(遺伝子組換え)製剤〕を指す。
*2 ICE:6ヵ月以前に治験薬投与を中止、12ヵ月以前に主要評価項目の評価に影響を及ぼす併用禁止薬を使用、ランダム化された治験薬ではなく、誤った治験薬投与を受けた、主要評価項目の評価に影響を及ぼす治験実施計画書からの逸脱と定義した。
*3 各有害事象はMedDRA v27.1に基づく。
*4 治験薬を1回以上投与したすべての患者
*5 ランダム化されたすべての患者のうち、投与量にかかわらず、1回以上の評価可能なPK パラメータを有する患者
*6 ランダム化されたすべての患者のうち、投与量にかかわらず、1回以上の評価可能なPDパラメータを有する患者
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
患者背景
ベースラインから12ヵ月時点までの人口統計学的特性(安全性解析対象集団)
| 項目 | 本剤60mg群 (n=266) | 先行バイオ医薬品群 (n=266) | |
|---|---|---|---|
| 年齢(歳)、平均値(SD) | 65.2(6.94) | 64.5(7.04) | |
| 閉経基準、n(%) | 自然閉経 | 243(91.4) | 244(91.7) |
| 臨床検査基準に基づく 閉経状態 | 9(3.4) | 8(3.0) | |
| 両側卵巣摘出術を施行 | 14(5.3) | 14(5.3) | |
| 人種、n(%) | 白人 | 246(92.5) | 249(93.6) |
| 黒人/アフリカ系アメリカ人 | 13(4.9) | 11(4.1) | |
| 複数人種* | 2(0.8) | 0 | |
| その他 | 5(1.9) | 6(2.3) | |
| 身長(cm)、平均値(SD) | 159.27(6.293) | 159.94(6.066) | |
| 体重(kg)、平均値(SD) | 63.71(9.552) | 64.49(10.040) | |
| BMI(kg/m2)、平均値(SD) | 25.12(3.547) | 25.20(3.605) | |
| 骨粗鬆症に対する生物学的製剤 による治療歴、n(%) | あり | 2(0.8) | 2(0.8) |
| なし | 264(99.2) | 264(99.2) | |
| 閉経からの経過年数、n(%) | 5年以下 | 20(7.5) | 20(7.5) |
| 5年超 | 246(92.5) | 246(92.5) | |
| 喫煙歴、n(%) | 喫煙歴なし | 209(78.6) | 211(79.3) |
| 喫煙歴あり | 33(12.4) | 25(9.4) | |
| 現喫煙者 | 24(9.0) | 30(11.3) | |
| 骨粗鬆症の診断からインフォームド・コンセント までの期間(月)、平均値(SD) | 23.4(41.75) | 26.8(49.77) | |
*「人種」の複数の項目に該当した場合、「複数人種」として集計した。
12ヵ月時点から18ヵ月時点までの人口統計学的特性(安全性解析対象集団)
| 項目 | 本剤60mg群 (n=242) | 先行バイオ医薬品 -本剤群 (n=122) | 先行バイオ医薬品 -継続群 (n=122) | |
|---|---|---|---|---|
| 年齢(歳)、平均値(SD) | 64.8(6.66) | 64.5(7.17) | 64.5(6.87) | |
| 閉経基準、n(%) | 自然閉経 | 222(91.7) | 112(91.8) | 113(92.6) |
| 臨床検査基準に基づく閉経状態 | 7(2.9) | 6(4.9) | 1(0.8) | |
| 両側卵巣摘出術を施行 | 13(5.4) | 4(3.3) | 8(6.6) | |
| 人種、n(%) | 白人 | 227(93.8) | 119(97.5) | 110(90.2) |
| 黒人/アフリカ系アメリカ人 | 8(3.3) | 3(2.5) | 7(5.7) | |
| 複数人種 | 2(0.8) | 0 | 0 | |
| その他 | 5(2.1) | 0 | 5(4.1) | |
| 身長(cm)、平均値(SD) | 159.51(6.246) | 160.51(5.918) | 159.41(6.292) | |
| 体重(kg)、平均値(SD) | 63.71(9.513) | 64.89(9.839) | 64.89(9.994) | |
| BMI(kg/m2)、平均値(SD) | 25.05(3.534) | 25.17(3.490) | 25.53(3.614) | |
| 骨粗鬆症に対する生物学的製剤による治療歴、n(%) | あり | 2(0.8) | 1(0.8) | 0 |
| なし | 240(99.2) | 121(99.2) | 122(100) | |
| 閉経からの経過年数、n(%) | 5年以下 | 19(7.9) | 9(7.4) | 9(7.4) |
| 5年超 | 223(92.1) | 113(92.6) | 113(92.6) | |
| 喫煙歴、n(%) | 喫煙歴なし | 191(78.9) | 98(80.3) | 97(79.5) |
| 喫煙歴あり | 28(11.6) | 14(11.5) | 9(7.4) | |
| 現喫煙者 | 23(9.5) | 10(8.2) | 16(13.1) | |
| 骨粗鬆症の診断からインフォームド・コンセントまでの期間(月)、平均値(SD) | 23.3(41.83) | 26.6(46.23) | 30.3(55.85) | |
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
12ヵ月時点での腰椎骨密度のベースラインからの変化率(主要評価項目)[検証的解析結果]
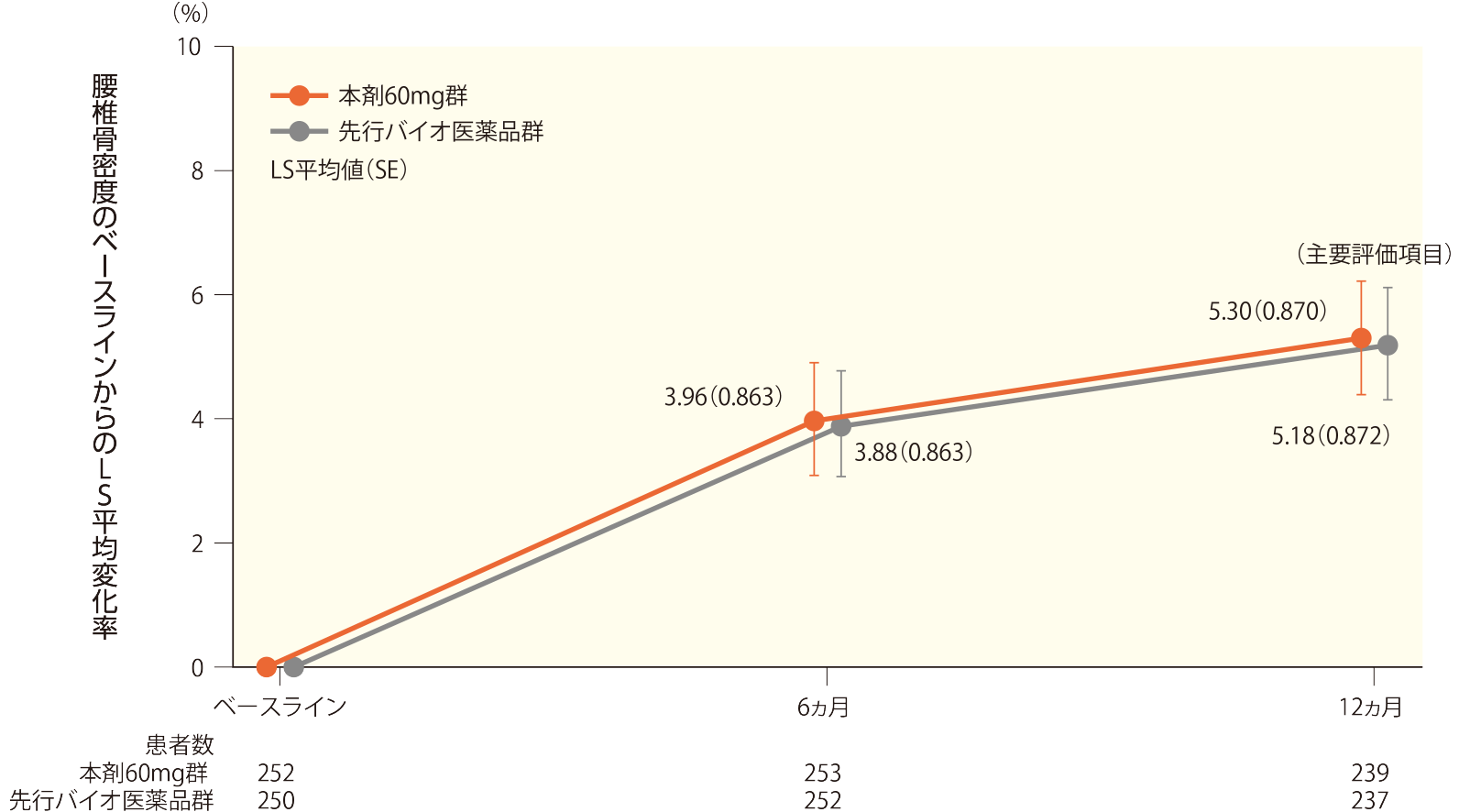
12ヵ月時点での腰椎骨密度のベースラインからの変化率のLS平均値(SE)は本剤60mg群で5.30(0.870)%、先行バイオ医薬品群で5.18(0.872)%、両群間の変化率のLS平均値の差(SE)は0.12(0.356)%であった。
両群間の変化率のLS平均値の差の95%信頼区間は(-0.58, 0.82)であり、事前に規定した同等性マージン(-1.45%, 1.45%)内に収まっていたことから、有効性の同等性が示された。
腰椎骨密度のベースラインからの変化率の推移(FAS)
| 本剤60mg群 (n=266) | 先行バイオ医薬品群 (n=266) | |
| 12ヵ月時点 | ||
| n | 239 | 237 |
| 腰椎骨密度のベースラインからの変化率*のLS平均値(SE)、% | 5.30 (0.870) | 5.18 (0.872) |
| 両群間の変化率のLS平均値の差(SE)、% | 0.12 (0.356) | |
| LS平均値の差の95%信頼区間 | -0.58, 0.82 | |
* 治療、来院、治療と来院の交互作用、骨粗鬆症に対する生物学的製剤による治療歴(あり/なし)をカテゴリー変数、ベースラインの骨密度及び閉経からの経過年数を連続共変量とするMMRMにより解析した。無構造の共分散構造により患者内誤差をモデル化し、Kenward-Roger近似により自由度を調整した。
12ヵ月時点における両群間の変化率のLS平均値の差(95%信頼区間)
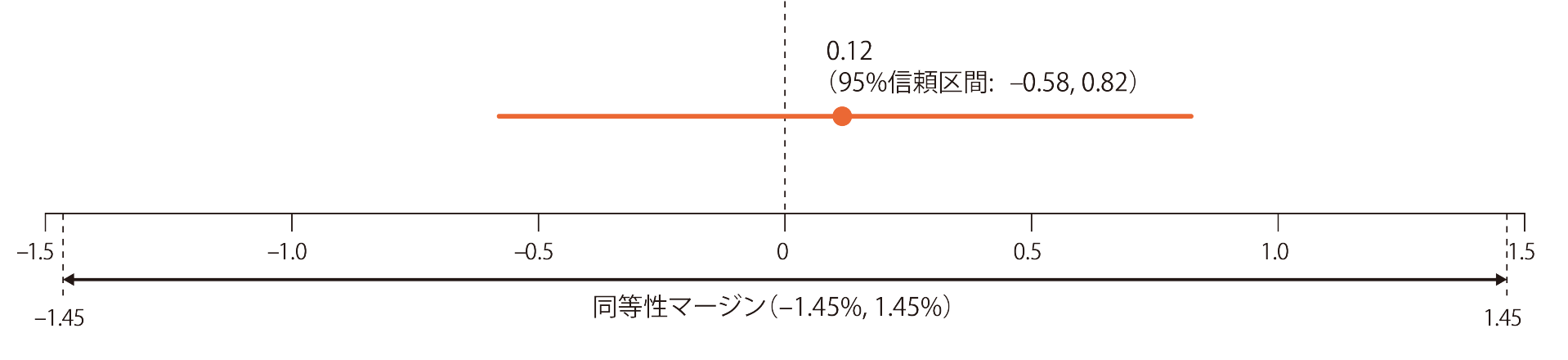
6及び18ヵ月時点での腰椎骨密度のベースラインからの変化率(副次評価項目)
(1)6ヵ月時点での腰椎骨密度のベースラインからの変化率
6ヵ月時点での腰椎骨密度のベースラインからの変化率のLS平均値(SE)は本剤60mg群で3.96(0.863)%、先行バイオ医薬品群で3.88(0.863)%、両群間の変化率のLS平均値の差(SE)は0.08(0.314)%であった。
腰椎骨密度のベースラインからの変化率(FAS)
| 本剤60mg群 (n=266) | 先行バイオ医薬品群 (n=266) | |
| 6ヵ月時点 | ||
| n | 253 | 252 |
| 腰椎骨密度のベースラインからの変化率*のLS平均値(SE)、% | 3.96 (0.863) | 3.88 (0.863) |
| 両群間の変化率のLS 平均値の差(SE)、% | 0.08 (0.314) | |
* 治療、来院、治療と来院の交互作用、骨粗鬆症に対する生物学的製剤による治療歴(あり/なし)をカテゴリー変数、ベースラインの骨密度及び閉経からの経過年数を連続共変量とするMMRMにより解析した。
(2)18ヵ月時点での腰椎骨密度のベースラインからの変化率
18ヵ月時点での腰椎骨密度のベースラインからの変化率のLS平均値(SE)は本剤60mg群で5.86(1.260)%、先行バイオ医薬品-本剤群で6.16(1.290)%、先行バイオ医薬品-継続群で5.58(1.310)%であった。
各群における変化率のLS平均値の差(SE)は、本剤60mg群と先行バイオ医薬品-本剤群で-0.29(0.485)%、本剤60mg群と先行バイオ医薬品-継続群で0.29(0.485)%、先行バイオ医薬品-本剤群と先行バイオ医薬品-継続群で0.58(0.559)%であった。
腰椎骨密度のベースラインからの変化率(FAS)
| 本剤60mg群 (n=242) | 先行バイオ医薬品 -本剤群 (n=122) | 先行バイオ医薬品 -継続群 (n=122) | |
| 18ヵ月時点 | |||
| n | 236 | 119 | 119 |
| 腰椎骨密度のベースラインからの変化率*のLS平均値(SE)、% | 5.86 (1.260) | 6.16 (1.290) | 5.58 (1.310) |
| 両群間の変化率のLS平均値の差(SE)、% |
| ||
* 治療、骨粗鬆症に対する生物学的製剤による治療歴(あり/なし)をカテゴリー変数、ベースラインの骨密度及び閉経からの経過年数を連続共変量とするANCOVAにより解析した。
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
6、12及び18ヵ月時点での大腿骨近位部(total hip)及び大腿骨頸部骨密度のベースラインからの変化率(副次評価項目)
(1)6及び12ヵ月時点でのtotal hip骨密度のベースラインからの変化率
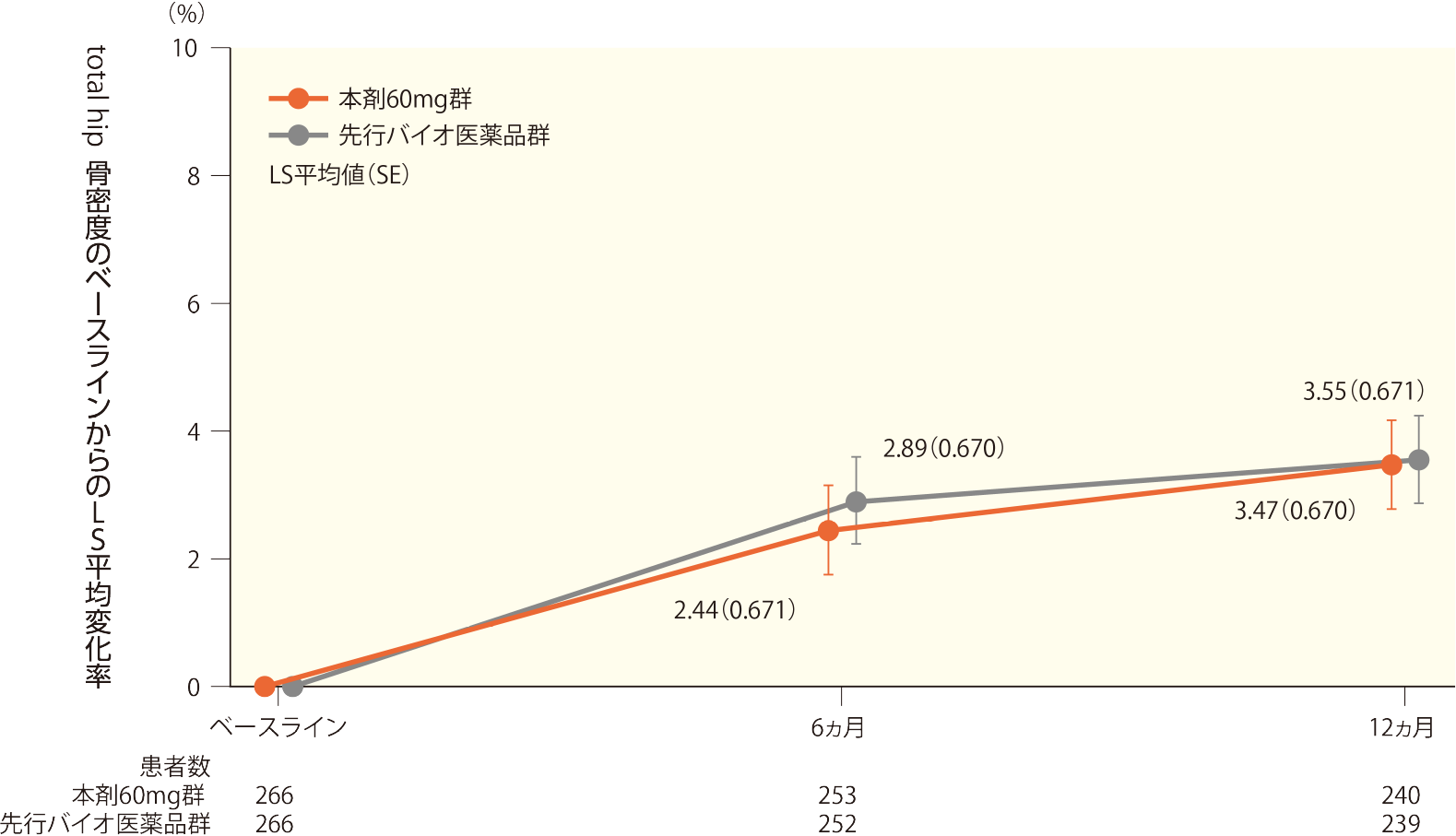
6ヵ月時点でのtotal hip骨密度のベースラインからの変化率のLS平均値(SE)は本剤60mg群で2.44(0.671)%、先行バイオ医薬品群で2.89(0.670)%、両群間の変化率のLS平均値の差(SE)は-0.45(0.253)%であった。
同様に、12ヵ月時点でのベースラインからの変化率のLS平均値(SE)は本剤60mg群で3.47(0.670)%、先行バイオ医薬品群で3.55(0.671)%、両群間の変化率のLS平均値の差(SE)は-0.08(0.247)%であった。
total hip骨密度のベースラインからの変化率の推移(FAS)
| 本剤60mg群 | 先行バイオ医薬品群 | |
| 6ヵ月時点 | ||
| n | 253 | 252 |
| total hip骨密度のベースラインからの変化率*のLS平均値(SE)、% | 2.44 (0.671) | 2.89 (0.670) |
| 両群間の変化率のLS平均値の差(SE)、% | -0.45 (0.253) | |
| 12ヵ月時点 | ||
| n | 240 | 239 |
| total hip骨密度のベースラインからの変化率*のLS平均値(SE)、% | 3.47 (0.670) | 3.55 (0.671) |
| 両群間の変化率のLS平均値の差(SE)、% | -0.08 (0.247) | |
* 治療、来院、治療と来院の交互作用、骨粗鬆症に対する生物学的製剤による治療歴(あり/なし)をカテゴリー変数、ベースラインの骨密度及び閉経からの経過年数を連続共変量とするMMRMにより解析した。
(2)18ヵ月時点でのtotal hip骨密度のベースラインからの変化率
18ヵ月時点での、各群におけるtotal hip骨密度のベースラインからの変化率のLS平均値の差(SE)は、本剤60mg群と先行バイオ医薬品-本剤群で-0.21(0.314)%、本剤60mg群と先行バイオ医薬品-継続群で0.29(0.313)%、先行バイオ医薬品-本剤群と先行バイオ医薬品-継続群で0.50(0.362)%であった。
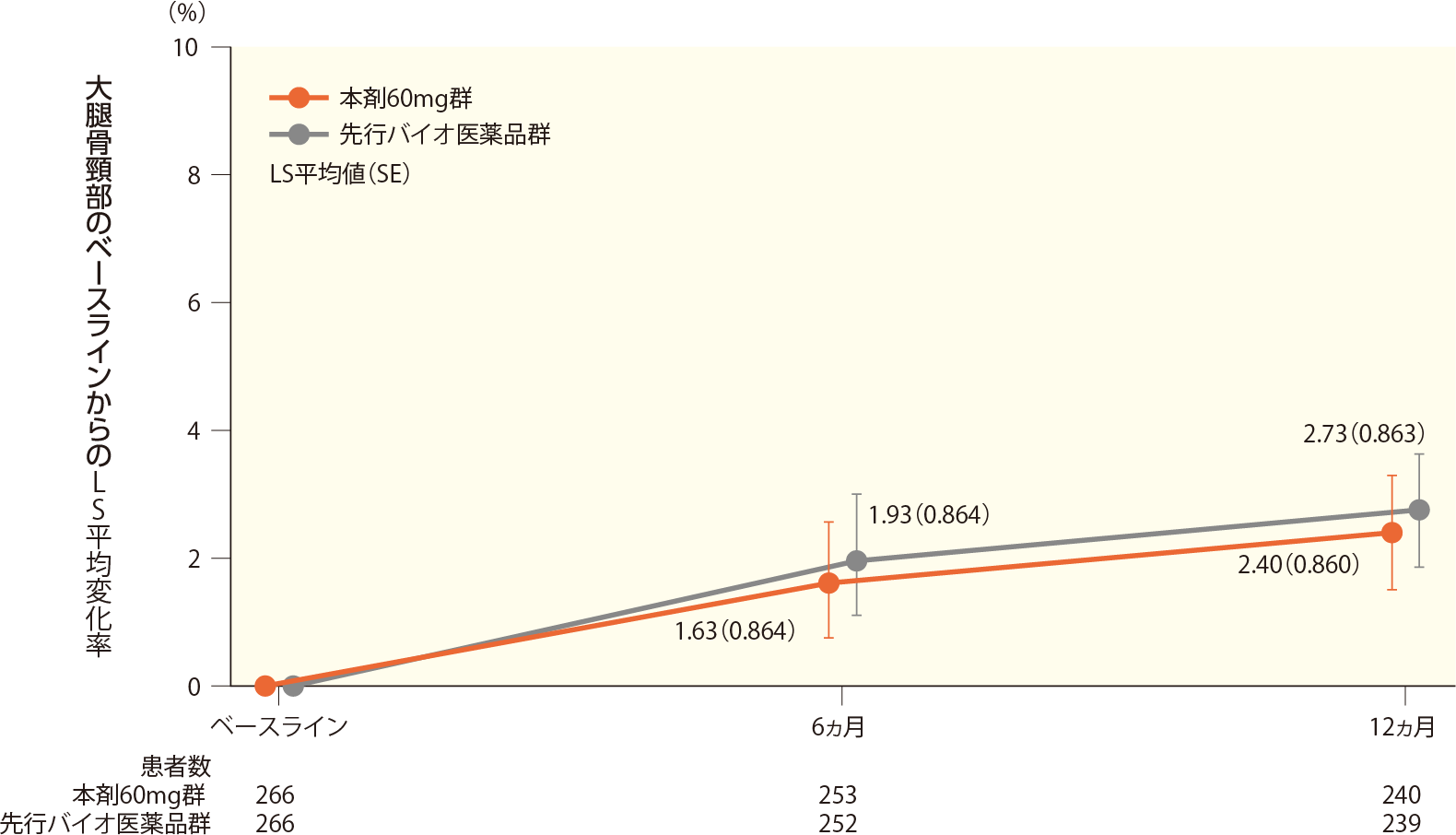
(3)6及び12ヵ月時点での大腿骨頸部骨密度のベースラインからの変化率
6ヵ月時点での大腿骨頸部骨密度のベースラインからの変化率のLS平均値(SE)は本剤60mg群で1.63(0.864)%、先行バイオ医薬品群で1.93(0.864)%、両群間の変化率のLS平均値の差(SE)は-0.30(0.337)%であった。
同様に、12ヵ月時点でのベースラインからの変化率のLS平均値(SE)は本剤60mg群で2.40(0.860)%、先行バイオ医薬品群で2.73(0.863)%、両群間の変化率のLS平均値の差(SE)は-0.33(0.316)%であった。
大腿骨頸部骨密度のベースラインからの変化率の推移(FAS)
| 本剤60mg群 | 先行バイオ医薬品群 | |
| 6ヵ月時点 | ||
| n | 253 | 252 |
| 大腿骨頸部骨密度のベースラインからの変化率*のLS平均値(SE)、% | 1.63 (0.864) | 1.93 (0.864) |
| 両群間の変化率のLS 平均値の差(SE)、% | -0.30 (0.337) | |
| 12ヵ月時点 | ||
| n | 240 | 239 |
| 大腿骨頸部骨密度のベースラインからの変化率*のLS平均値(SE)、% | 2.40 (0.860) | 2.73 (0.863) |
| 両群間の変化率のLS 平均値の差(SE)、% | -0.33 (0.316) | |
* 治療、来院、治療と来院の交互作用、骨粗鬆症に対する生物学的製剤による治療歴(あり/なし)をカテゴリー変数、ベースラインの骨密度及び閉経からの経過年数を連続共変量とするMMRMにより解析した。
(4)18ヵ月時点での大腿骨頸部骨密度のベースラインからの変化率
18ヵ月時点での、各群における大腿骨頸部骨密度のベースラインからの変化率のLS平均値の差(SE)は、本剤60mg群と先行バイオ医薬品-本剤群で0.58(0.430)%、本剤60mg群と先行バイオ医薬品- 継続群で0.43(0.430)%、先行バイオ医薬品-本剤群と先行バイオ医薬品-継続群で-0.15(0.496)%であった。
12及び18ヵ月時点での新規椎体形態骨折の発現頻度(副次評価項目)
(1)12ヵ月時点での新規椎体形態骨折の発現頻度
12ヵ月時点までに、新規椎体形態骨折は本剤60mg群で8例(3.3%)、先行バイオ医薬品群で6例(2.5%)に認められた。
12ヵ月時点での新規椎体形態骨折の発現頻度(FAS)
| 本剤60mg群 (n=266) | 先行バイオ医薬品群 (n=266) | |
| 12ヵ月時点 | ||
| n | 241 | 242 |
| 新規椎体形態骨折が認められた患者、n(%) | 8 (3.3) | 6 (2.5) |
(2)12ヵ月時点から18ヵ月時点までの新規椎体形態骨折の発現頻度
12ヵ月時点から18ヵ月時点までに、新規椎体形態骨折は本剤60mg群で4例(1.7%)、先行バイオ医薬品-本剤群で1例(0.9%)、先行バイオ医薬品-継続群で1例(0.9%)に認められた。
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
安全性
(1)12ヵ月時点までの安全性
主な副作用
副作用は本剤60mg群では266例中59例(22.2%)、先行バイオ医薬品群では266例中50例(18.8%)に認められた。主な副作用(3%以上に発現)は、本剤60mg群では低カルシウム血症24例(9.0%)、補正カルシウム減少11例(4.1%)、注射部位反応9例(3.4%)、先行バイオ医薬品群では低カルシウム血症18例(6.8%)、注射部位反応8例(3.0%)であった。
副作用(いずれかの群で1%以上に発現)(安全性解析対象集団)
| 本剤60mg群 (n=266) | 先行バイオ医薬品群 (n=266) | |
| n(%) | n(%) | |
| 副作用発現例 | 59 (22.2) | 50 (18.8) |
| 代謝および栄養障害 | 24 (9.0) | 19 (7.1) |
| 低カルシウム血症 | 24 (9.0) | 18 (6.8) |
| 筋骨格系および結合組織障害 | 13 (4.9) | 17 (6.4) |
| 筋骨格痛 | 6 (2.3) | 7 (2.6) |
| 関節痛 | 3 (1.1) | 4 (1.5) |
| 四肢痛 | 3 (1.1) | 2 (0.8) |
| 臨床検査 | 18 (6.8) | 9 (3.4) |
| 補正カルシウム減少 | 11 (4.1) | 3 (1.1) |
| 活性化部分トロンボプラスチン時間延長 | 6 (2.3) | 2 (0.8) |
| カルシウムイオン減少 | 3 (1.1) | 3 (1.1) |
| 一般・全身障害および投与部位の状態 | 12 (4.5) | 8 (3.0) |
| 注射部位反応 | 9 (3.4) | 8 (3.0) |
MedDRA v27.1
重篤な有害事象
重篤な有害事象は本剤60mg群では9例(3.4%)、先行バイオ医薬品群では10例(3.8%)に認められた。内訳は、本剤60mg群では慢性胃炎、びらん性十二指腸炎、膵炎、感染性筋炎、肺炎、軟部組織感染、遠隔転移を伴う肺癌、慢性冠症候群、心室性不整脈、死亡、原発性副甲状腺機能亢進症、脱水、腎不全、性器脱各1例(0.4%)、先行バイオ医薬品群では腹痛、虫垂炎、女性乳癌、骨血管腫、突然死、抑うつ気分、統合失調感情障害、高血圧、腸骨動脈閉塞、頭蓋脳損傷各1例(0.4%)であった。
早期試験中止又は投与中止に至った有害事象
早期試験中止又は投与中止に至った有害事象は本剤60mg群では8例(3.0%)、先行バイオ医薬品群では3例(1.1%)に認められた。内訳は、本剤60mg群では関節痛、顎痛、脊椎痛、死亡、原発性副甲状腺機能亢進症、糸球体濾過率減少、腎不全、脱毛症各1例(0.4%)、先行バイオ医薬品群では突然死、過敏症、顎膿瘍各1例(0.4%)であった。
死亡に至った有害事象
死亡に至った有害事象は本剤60mg群では3例(1.1%)、先行バイオ医薬品群では1例(0.4%)に認められた。内訳は、本剤60mg群では肺炎、遠隔転移を伴う肺癌、死亡(原因不明)各1例(0.4%)、先行バイオ医薬品群では突然死1例(0.4%)であった。
(2)12ヵ月時点から18ヵ月時点までの安全性
主な副作用
副作用は本剤60mg群では242例中16例(6.6%)、先行バイオ医薬品-本剤群では122例中4例(3.3%)、先行バイオ医薬品-継続群では122例中5例(4.1%)に認められた。主な副作用(1%以上に発現)は、本剤60mg群では補正カルシウム減少8例(3.3%)、カルシウムイオン減少5例(2.1%)、先行バイオ医薬品-本剤群では補正カルシウム減少2例(1.6%)、先行バイオ医薬品-継続群ではカルシウムイオン減少2例(1.6%)であった。
副作用(いずれかの群で1%以上に発現)(安全性解析対象集団)
| 本剤60mg群 (n=242) | 先行バイオ医薬品 -本剤群 (n=122) | 先行バイオ医薬品 -継続群 (n=122) | |
| n(%) | n(%) | n(%) | |
| 副作用発現例 | 16 (6.6) | 4 (3.3) | 5 (4.1) |
| 臨床検査 | 11 (4.5) | 3 (2.5) | 3 (2.5) |
| 補正カルシウム減少 | 8 (3.3) | 2 (1.6) | 0 |
| カルシウムイオン減少 | 5 (2.1) | 1 (0.8) | 2 (1.6) |
MedDRA v27.1
重篤な有害事象
重篤な有害事象は本剤60mg群で6例(2.5%)、先行バイオ医薬品-本剤群で3例(2.5%)、先行バイオ医薬品-継続群で2例(1.6%)に認められた。内訳は、本剤60mg群では汎⾎球減少症、急性腎盂腎炎、前腕骨折、複視、腸閉塞、突然死各1例(0.4%)、先行バイオ医薬品-本剤群では鉄欠乏性貧血、大腿骨骨折、両耳難聴各1例(0. 8%)、先行バイオ医薬品-継続群では虫垂炎、うっ血性心不全、胆嚢炎各1例(0. 8%)であった。
早期試験中止又は投与中止に至った有害事象
早期試験中止又は投与中止に至った有害事象はいずれの群においても認められなかった。
死亡に至った有害事象
死亡に至った有害事象は本剤60mg群では突然死が1例(0.4%)に認められた。先行バイオ医薬品-本剤群、先行バイオ医薬品-継続群では死亡に至った有害事象は認められなかった。
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
投与前、1日、2日、12日、30日、60日、90日、180日、270日、12ヵ月、12ヵ月+2週、15ヵ月及び18ヵ月時点での抗薬物抗体(ADA)及び中和抗体(nAb)発現頻度(副次評価項目)
(1)12ヵ月時点までのADA及びnAb発現頻度
治験薬投与下で発現したADAは、本剤60mg群で256例中256例(100.0%)、先行バイオ医薬品群で251例中251例(100.0%)に認められた。
同様に、治験薬投与下で発現したnAbは、本剤60mg群で13例(5.1%)、先行バイオ医薬品群で19例(7.6%)に認められた。
時期別ADA発現頻度
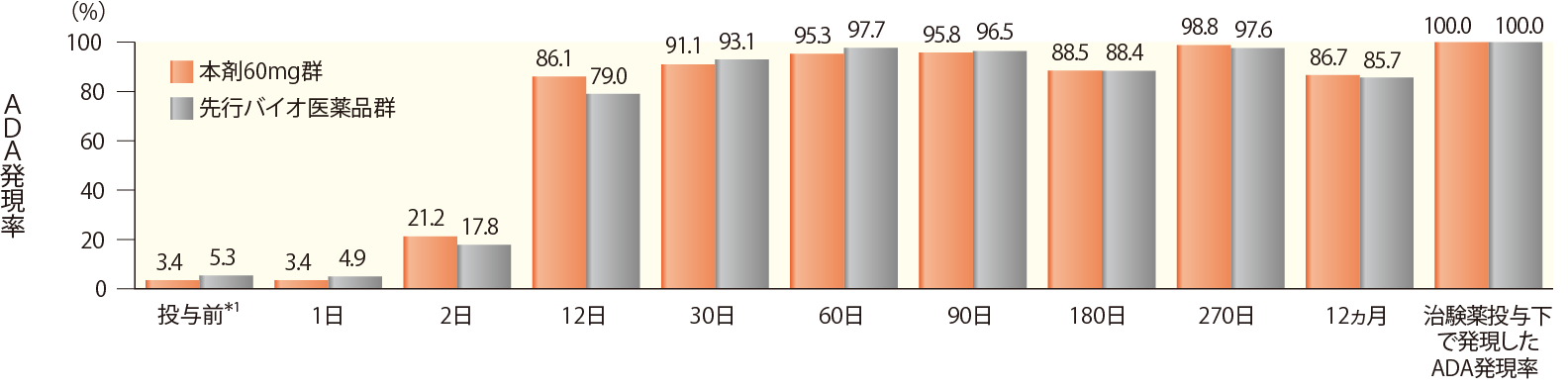
| 投与前*1 | 1日 | 2日 | 12日 | 30日 | 60日 | 90日 | 180日 | 270日 | 12ヵ月 | 治験薬 投与下で 発現した ADA 発現率 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 本剤 60mg群 | 9*2/264 (3.4) | 9/265 (3.4) | 56/264 (21.2) | 217/252 (86.1) | 236/259 (91.1) | 246/258 (95.3) | 251/262 (95.8) | 224/253 (88.5) | 242/245 (98.8) | 209/241 (86.7) | 256/256 (100.0) |
| 先行バイオ 医薬品群 | 14*2/264 (5.3) | 13/265 (4.9) | 47/264 (17.8) | 207/262 (79.0) | 241/259 (93.1) | 250/256 (97.7) | 249/258 (96.5) | 221/250 (88.4) | 241/247 (97.6) | 209/244 (85.7) | 251/251 (100.0) |
*1 ベースライン
*2 pre-existing antibody(既存抗体)といった交差反応性の抗体を有する患者。
表中の数字はADA陽性例数/評価例数(発現率)を示す。
時期別nAb発現頻度
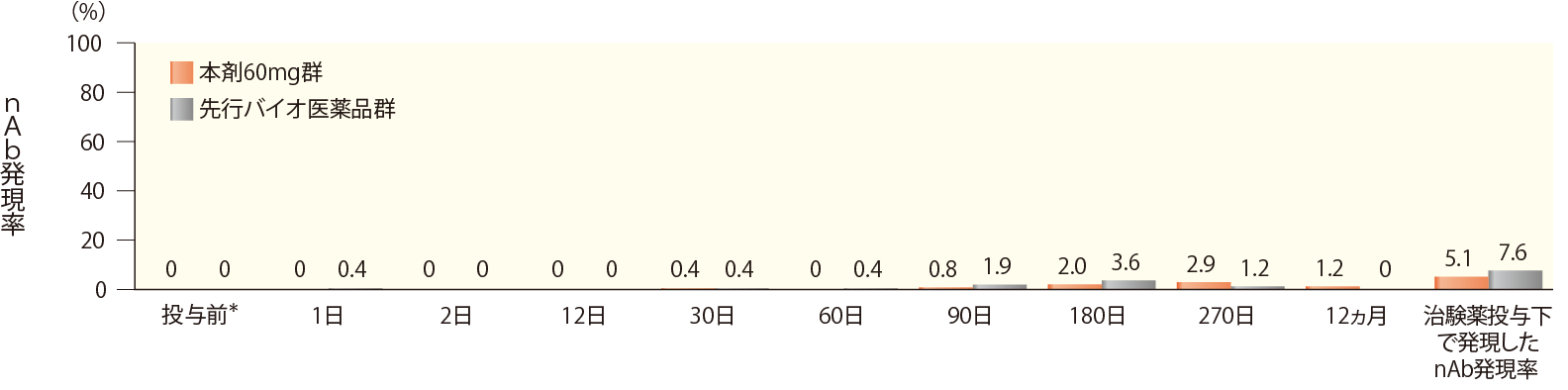
| 投与前* | 1日 | 2日 | 12日 | 30日 | 60日 | 90日 | 180日 | 270日 | 12ヵ月 | 治験薬 投与下で 発現した nAb 発現率 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 本剤 60mg群 | 0/264 (0) | 0/265 (0) | 0/264 (0) | 0/252 (0) | 1/259 (0.4) | 0/258 (0) | 2/262 (0.8) | 5/253 (2.0) | 7/245 (2.9) | 3/241 (1.2) | 13/256 (5.1) |
| 先行バイオ 医薬品群 | 0/264 (0) | 1/265 (0.4) | 0/264 (0) | 0/262 (0) | 1/259 (0.4) | 1/256 (0.4) | 5/258 (1.9) | 9/250 (3.6) | 3/247 (1.2) | 0/244 (0) | 19/251 (7.6) |
*ベースライン
表中の数字はnAb陽性例数/評価例数(発現率)を示す。
(2)12ヵ月時点から18ヵ月時点までのADA及びnAb発現頻度
ADAは本剤60mg群で237例中215例(90.7%)、先行バイオ医薬品-本剤群で119例中111例(93.3%)、先行バイオ医薬品-継続群で118例中109例(92.4%)に認められた。
同様に、nAbは本剤60mg群で2例(0.8%)、先行バイオ医薬品-本剤群で1例(0.8%)、先行バイオ医薬品-継続群で1例(0.8%)に認められた。
時期別ADA発現頻度
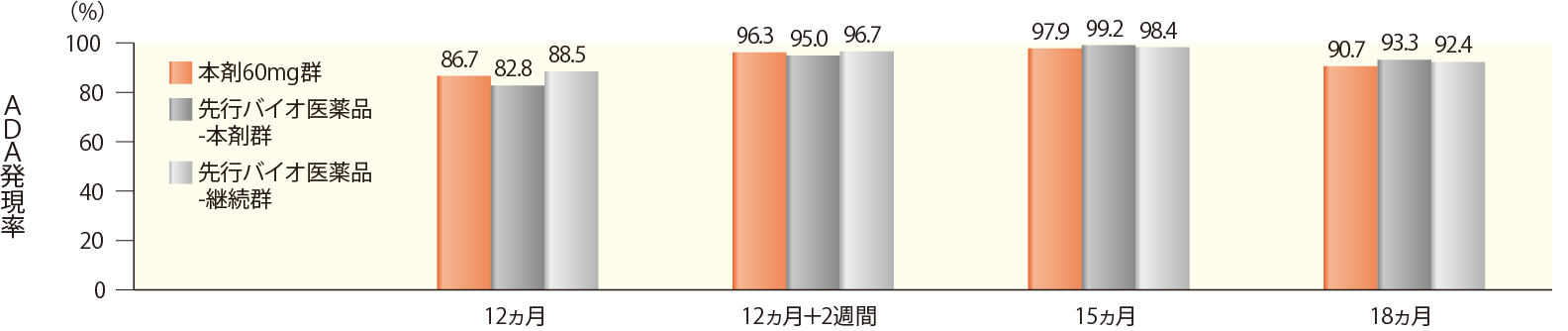
| 12ヵ月 | 12ヵ月+2週間 | 15ヵ月 | 18ヵ月 | |
|---|---|---|---|---|
| 本剤60mg群 | 209/241 (86.7) | 233/242 (96.3) | 235/240 (97.9) | 215/237 (90.7) |
| 先行バイオ医薬品 -本剤群 | 101/122 (82.8) | 114/120 (95.0) | 119/120 (99.2) | 111/119 (93.3) |
| 先行バイオ医薬品 -継続群 | 108/122 (88.5) | 118/122 (96.7) | 120/122 (98.4) | 109/118 (92.4) |
表中の数字はADA陽性例数/評価例数(発現率)を示す。
時期別nAb発現頻度
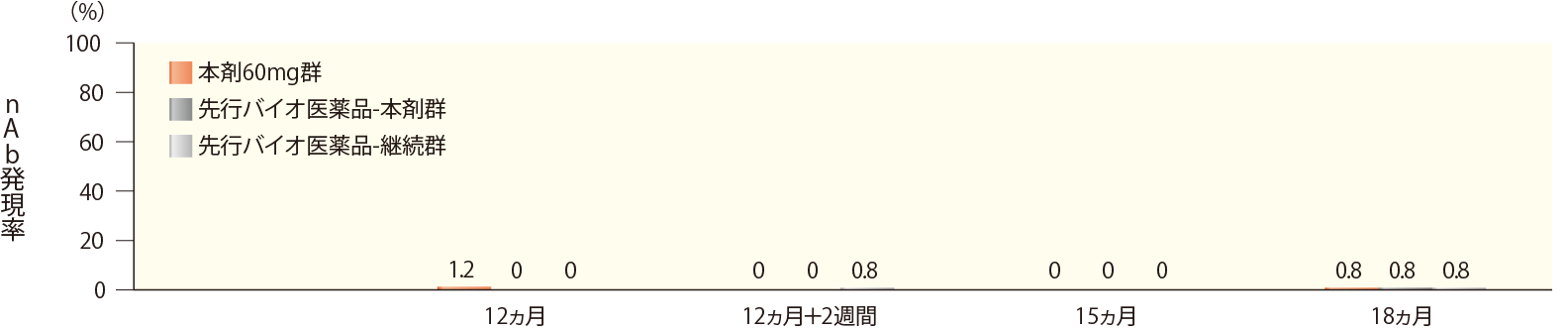
| 12ヵ月 | 12ヵ月+2週間 | 15ヵ月 | 18ヵ月 | |
|---|---|---|---|---|
| 本剤60mg群 | 3/241 (1.2) | 0/242 (0) | 0/240 (0) | 2/237 (0.8) |
| 先行バイオ医薬品 -本剤群 | 0/122 (0) | 0/120 (0) | 0/120 (0) | 1/119 (0.8) |
| 先行バイオ医薬品 -継続群 | 0/122 (0) | 1/122 (0.8) | 0/122 (0) | 1/118 (0.8) |
表中の数字はnAb陽性例数/評価例数(発現率)を示す。
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
3、6、9、12及び18ヵ月時点での血清中I型コラーゲン架橋C-テロペプチド(sCTX-1)のベースラインからの変化率(副次評価項目)
(1)3、6、9及び12ヵ月時点でのsCTX-1のベースラインからの変化率
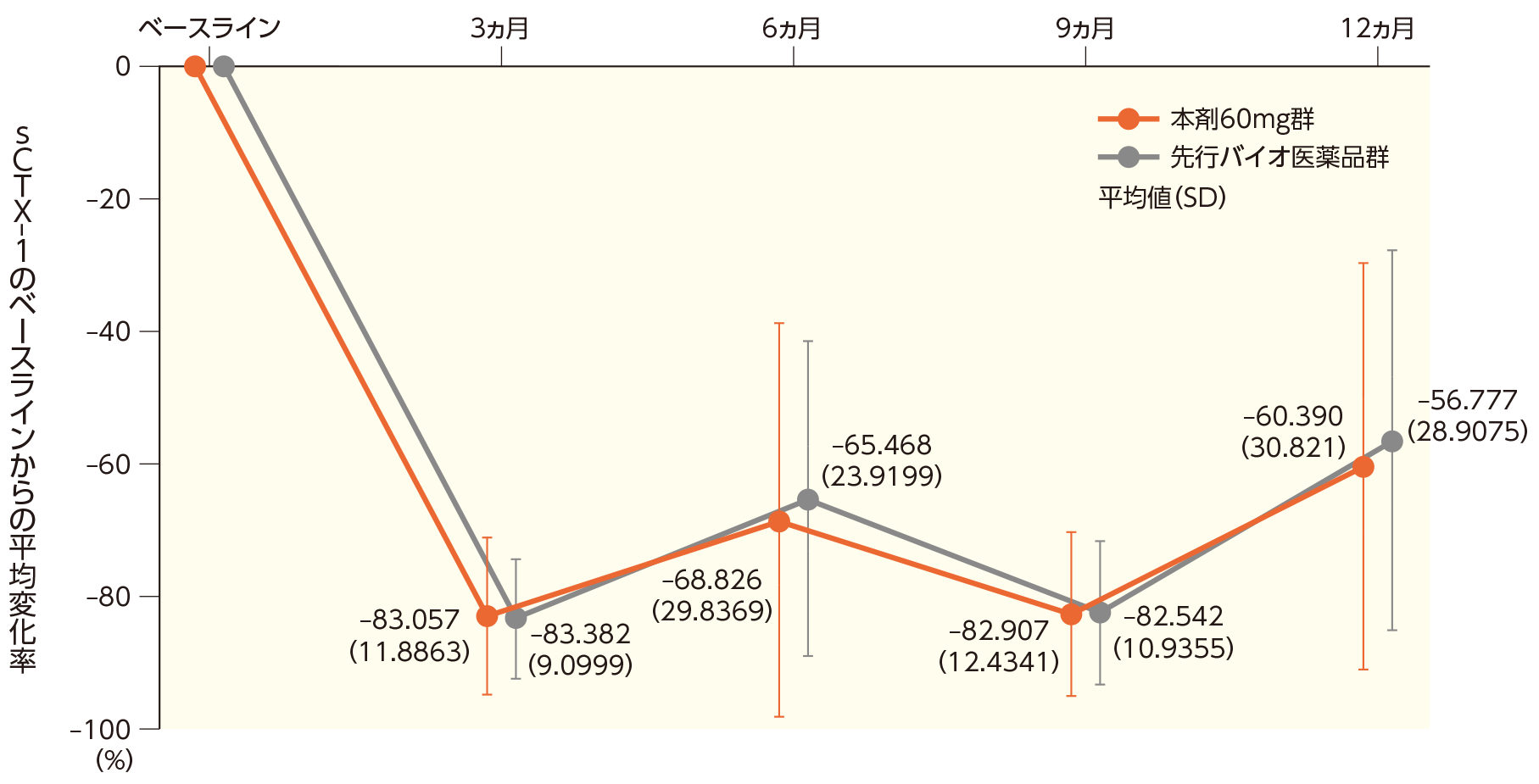
本剤60mg群及び先行バイオ医薬品群におけるsCTX-1のベースラインからの変化率は以下のとおりであった。
sCTX-1のベースラインからの変化率の推移(PD解析対象集団)
| 本剤60mg群 | 先行バイオ医薬品群 | |
| 3ヵ月時点 | ||
| n | 259 | 257 |
| sCTX-1のベースラインからの変化率の平均値(SD)、% | -83.057(11.8863) | -83.382(9.0999) |
| 6ヵ月時点 | ||
| n | 250 | 250 |
| sCTX-1のベースラインからの変化率の平均値(SD)、% | -68.826(29.8369) | -65.468(23.9199) |
| 9ヵ月時点 | ||
| n | 241 | 245 |
| sCTX-1のベースラインからの変化率の平均値(SD)、% | -82.907(12.4341) | -82.542(10.9355) |
| 12ヵ月時点 | ||
| n | 236 | 242 |
| sCTX-1のベースラインからの変化率の平均値(SD)、% | -60.390(30.8218) | -56.777(28.9075) |
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
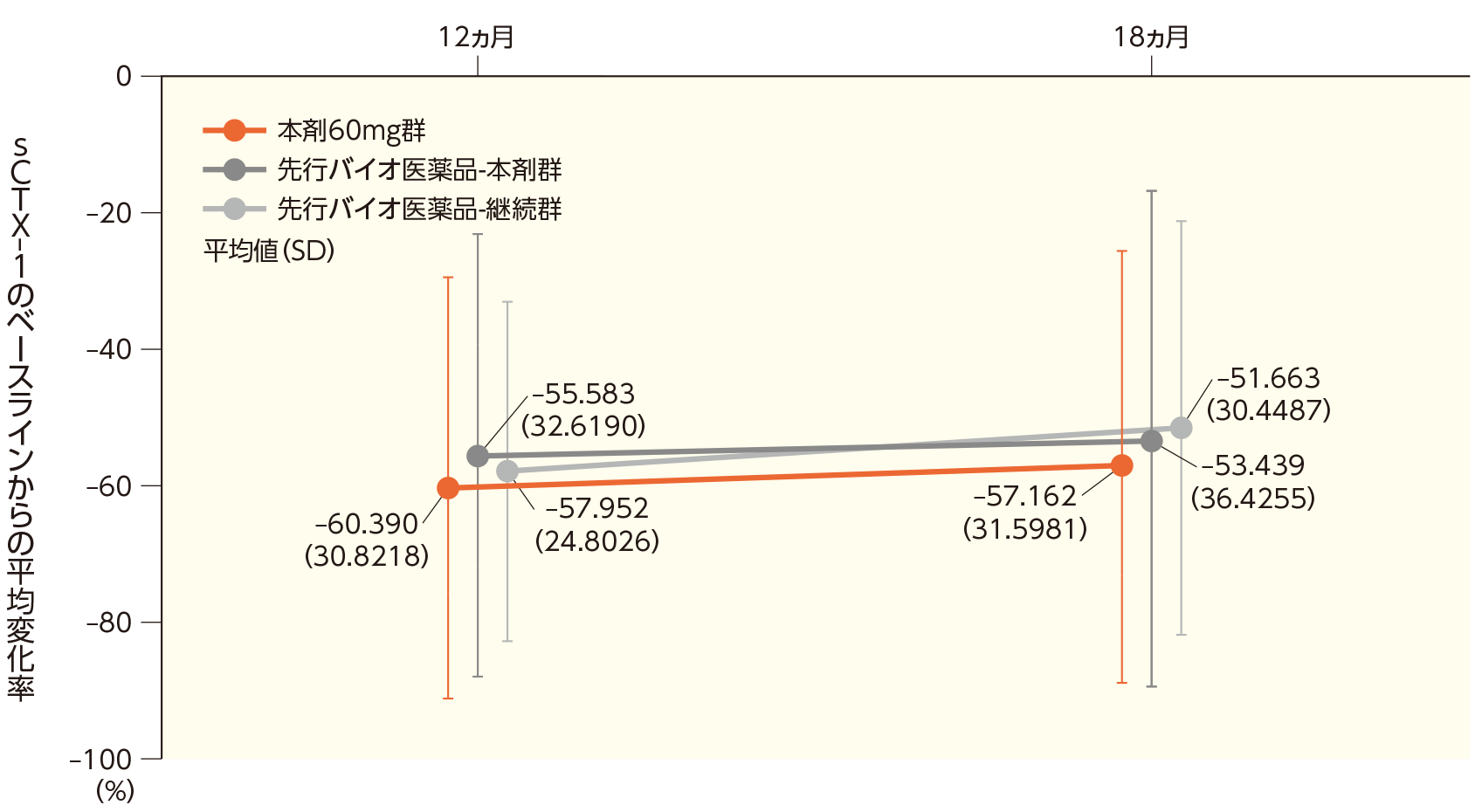
(2)12及び18ヵ月時点でのsCTX-1のベースラインからの変化率
本剤60mg群、先行バイオ医薬品-本剤群、先行バイオ医薬品-継続群におけるsCTX-1のベースラインからの変化率は以下のとおりであった。
sCTX-1のベースラインからの変化率の推移(PD解析対象集団)
| 本剤60mg群 | 先行バイオ医薬品-本剤群 | 先行バイオ医薬品-継続群 | |
| 12ヵ月時点 | |||
| n | 236 | 120 | 122 |
| sCTX-1のベースラインからの 変化率の平均値(SD)、% | -60.390(30.8218) | -55.583(32.6190) | -57.952(24.8026) |
| 18ヵ月時点 | |||
| n | 233 | 116 | 118 |
| sCTX-1のベースラインからの 変化率の平均値(SD)、% | -57.162(31.5981) | -53.439(36.4255) | -51.663(30.4487) |
6ヵ月時点までのsCTX-1のベースラインからの変化率の効果曲線下面積(%CfbsCTX-1のAUEC0-6months)(副次評価項目)
6ヵ月時点までのsCTX-1のベースラインからの変化率の幾何平均値は本剤60mg群で2361.29h・%、先行バイオ医薬品群で2327.63h・%であった。
%Cfb sCTX-1のAUEC0-6months(ICEsの影響を受けたデータを除外)(PK解析対象集団)
| 本剤60mg群 | 先行バイオ医薬品群 | |
| 6ヵ月時点 | ||
| n | 243 | 248 |
| 幾何平均値、h・% | 2361.29 | 2327.63 |
- 社内資料:臨床試験の経緯[承認時評価資料]
- 社内資料:海外第Ⅲ相臨床試験成績(AVT03-GL-C01)[承認時評価資料]
- Lortkipanidze M, et al.: Expert Opin Biol Ther. 2025; 25(8): 899-912
- Bolognese MA, et al.: J Clin Densitom. 2013; 16(2): 147-153
- Orwoll E, et al.: J Clin Endocrinol Metab. 2012; 97(9): 3161-3169
- Bone HG, et al.: J Clin Endocrinol Metab. 2008; 93(6): 2149-2157
- Cummings SR, et al.: N Engl J Med. 2009; 361(8): 756-765
- McClung MR, et al.: N Engl J Med. 2006; 354(8): 821-831
- Meltone 3rd LJ, et al.: J Bone Miner Res. 1992; 7(9): 1005-1010
- Agrawal AC, et al.: Indian J Orthop. 2023; 57(Suppl1): 45-48
- Kanis JA, et al.: Osteoporos Int. 2019; 30(1): 3-44


