デノスマブとは
開発の経緯
デノスマブは特異的かつ高い親和性で核内因子-κB(NF-κB)活性化受容体(RANK)リガンド(RANKL)に結合するヒト型免疫グロブリンG2(IgG2)モノクローナル抗体である。デノスマブは、RANK/RANKL経路を阻害することにより破骨細胞の活性化を阻害することで、がんによる骨病変の進展を抑制すると考えられる。
デノスマブBS皮下注120mgRM「F」〔一般名:デノスマブ(遺伝子組換え)[デノスマブ後続1]、以下、本剤〕は、先行バイオ医薬品ランマーク®皮下注120mgのバイオ後続品(バイオシミラー)としてAlvotech社により開発された。
2024年10月に本剤の製造販売承認申請を行い、2025年9月に承認を取得した。
【デノスマブBS皮下注120mgRM「F」の効能又は効果】
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
特性
製品の治療学的特性
1.
本剤はデノスマブ(遺伝子組換え)の120mg含有製剤のバイオ後続品(バイオシミラー)である。
2.
閉経後骨粗鬆症患者(女性)を対象とした海外第Ⅲ相臨床試験(AVT03-GL-C01試験)により、先行バイオ医薬品(US)の60mg製剤※1との臨床的同等性が確認された(検証的解析結果)※2。
3.
重大な副作用として、低カルシウム血症(5.6%)、顎骨壊死・顎骨骨髄炎(1.8%)、アナフィラキシー(頻度不明)、大腿骨転子下・近位大腿骨骨幹部・近位尺骨骨幹部等の非定型骨折(頻度不明)、治療中止後の多発性椎体骨折(頻度不明)、重篤な皮膚感染症(0.1%)が報告されている※3。
なお、主な副作用として、貧血、頭痛、悪心、関節痛が報告されている。
詳細については電子添文の副作用及び臨床成績の安全性の結果を参照すること。
製品の製剤学的特性
1.
RANKLに結合する遺伝子組換え完全ヒト免疫グロブリンG2(IgG2)モノクローナル抗体であるデノスマブとして日本初のバイオシミラーである。
※1 先行バイオ医薬品(US)の60mg製剤は米国で承認されているプラリア®〔デノスマブ(遺伝子組換え)製剤〕を指す。
※2 製品の治療学的特性2の臨床試験は、本剤の効能又は効果とは異なる患者を対象に、国内未承認である本剤の皮下投与用プレフィルドシリンジ(PFS)製剤を用いて実施した。
※3 重大な副作用の発現頻度は先行バイオ医薬品(ランマーク®)の臨床試験結果に基づく副作用発現頻度である。
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
有効成分に関する理化学的知見
一般名:
デノスマブ(遺伝子組換え)[デノスマブ後続1](JAN)
分子量:
約147,000
本 質:
デノスマブ[デノスマブ後続1 ](以下、デノスマブ後続1)は、遺伝子組換え抗NF-κB 活性化受容体リガンド(RANKL)モノクローナル抗体であり、ヒトIgG2に由来する。
デノスマブ後続1は、CHO細胞により産生される。
デノスマブ後続1は、448個のアミノ酸残基からなるH鎖(γ2鎖)2本及び215個のアミノ酸残基からなるL鎖(κ鎖)2本で構成される糖タンパク質(分子量:約147,000)である。
分子式:
C6404H9908N1724O2004S50(タンパク質部分、4本鎖)
H鎖C2171H3349N575O671S20
L鎖C1031H1611N287O331S5
薬物動態
1.血清中濃度
(1)単回投与
1)日本人及び外国人健康成人男性への単回投与時の薬物動態(AVT03-GL-P03試験)1)(日本人及び外国人データ)
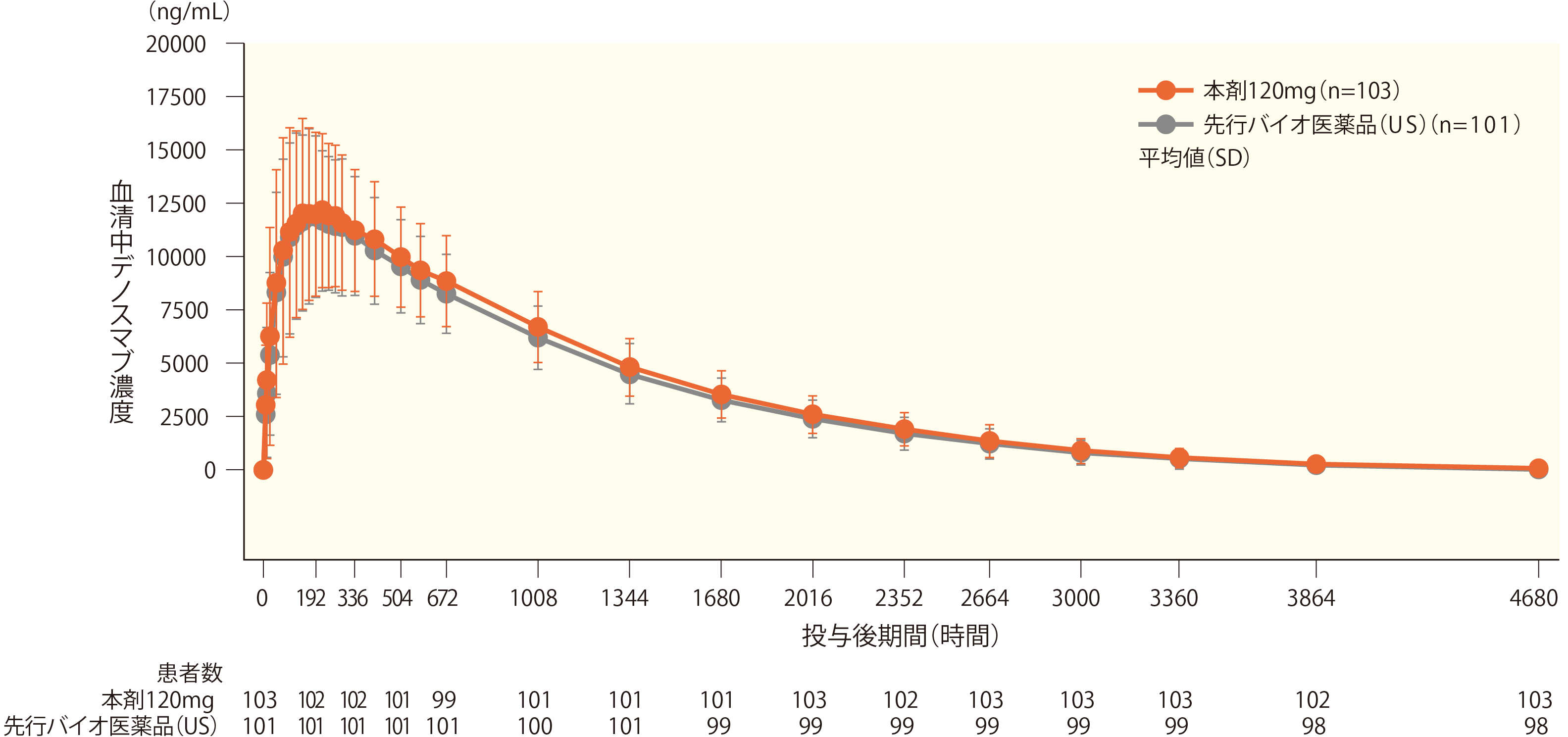
海外において、日本人24例を含む28-55歳の健康男性204例に、本剤120mg又は先行バイオ医薬品(US)の120mg製剤*を単回皮下投与したときの血清中濃度の推移及び薬物動態(PK)パラメータを以下に示す。
本剤120mgと先行バイオ医薬品(US)の120mg製剤投与時における0時間から定量下限を超える濃度を示す最終時点tまでの効果-時間曲線下面積(AUC0-t)の幾何平均値の比は107.80(1.032)%、最高血清中濃度(Cmax)の幾何平均値の比は103.96(1.035)%であった。これらの幾何平均値の比の90%信頼区間は、いずれも事前に定めた同等性マージン(80%, 125%)内に収まっていたことから、本剤120mgと先行バイオ医薬品(US)の120mg製剤との同等性が示された。
*先行バイオ医薬品(US)の120mg製剤は米国で承認されているランマーク®〔デノスマブ(遺伝子組換え)製剤〕を指す。
| AUC0-t (時間·μg/mL) | Cmax (μg/mL) | tmax (時間) | t1/2 (時間) | |
|---|---|---|---|---|
| 本剤120mg (n=103) | 16,052 (4,216) | 13.5 (4.6) | 216 (24~1,009) | 363.71 (169.44) |
| 先行バイオ医薬品(US) (n=101) | 14,943 (4,164) | 12.9 (4.3) | 192 (48~504) | 358.08 (193.64) |
AUC0-t:0時間から定量下限を超える濃度を示す最終時点tまでの効果-時間曲線下面積、Cmax:最高血清中濃度、tmax:最高血清中濃度到達時間、t1/2:消失半減期 tmax:中央値(範囲)、その他の項目:平均値(SD)
【デノスマブBS皮下注120mgRM「F」の効能又は効果、用法及び用量】
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
| 幾何平均値 | 最小二乗平均値(SE) | 幾何平均値の比 (SE)(%) | 90%信頼区間 (%)*1,2 | |
|---|---|---|---|---|
| AUC0-t (時間·ng/mL) | ||||
| 本剤120mg (n=103) | 15501387.91 | 15494141.60 (1.023) | 107.80 (1.032) | 102.298~113.600 |
| 先行バイオ医薬品(US) (n=101) | 14366056.19 | 14372907.99 (1.023) | ||
| Cmax(ng/mL) | ||||
| 本剤120mg (n=103) | 12761.45 | 12753.67 (1.024) | 103.96 (1.035) | 98.257~110.000 |
| 先行バイオ医薬品(US) (n=101) | 12259.85 | 12267.48 (1.025) | ||
*1 AUC0-t又はCmaxの自然対数変換値をもとに、投与群を固定効果とし、ベースラインの体重を連続共変量とした共分散分析モデルにより算出した。
*2 幾何平均値の比の90%信頼区間が、事前に規定した範囲(80%, 125%)の同等性マージン内に収まっている場合、同等性が示されたと判断した。
2)日本人骨転移患者への単回投与時の薬物動態
※デノスマブBS皮下注120mgRM「F」電子添文より
日本人乳癌骨転移患者に本剤60mg及び180mg注)を単回皮下投与したときの薬物動態パラメータを表に示す。
血清中デノスマブのCmax及びAUCは、60~180mgの用量範囲でほぼ用量に比例して増加した2)。
| 投与量 (mg) | n | Cmax (ng/mL) | Tmaxa) (日) | AUC0-t (μg・日/mL) | t1/2β (日) |
|---|---|---|---|---|---|
| 60 | 6 | 7,730±3,130 | 8(7~28) | 351±144 | 24.7±2.44 |
| 180 | 6 | 31,100±14,900 | 10(4~28) | 1,320±640 | 29.1±7.15 |
mean±SD
a)中央値(最小値~最大値)
注)ランマーク®の承認された用量は120mgである*。
3)閉経後の日本人健康成人女性への単回投与時の薬物動態
健康な日本人閉経後女性に本剤0.03、0.1、0.3、1.0及び3.0mg/kg注)を単回皮下投与したとき、デノスマブは0.03~3.0mg/kgの用量範囲で非線形の薬物動態を示したが、1.0及び3.0mg/kgではCmax及びAUCはほぼ用量に比例して増加した3,4) 。
| 投与量 (mg/kg) | n | Cmax (ng/mL) | Tmaxa) (日) | AUC0-t (μg・日/mL) |
|---|---|---|---|---|
| 0.03 | 6 | 99.6±25.8 | 7.00(7~10) | 2.06±0.53 |
| 0.1 | 6 | 492±166 | 12.0(7~21) | 15.2±6.7 |
| 0.3 | 6 | 1,910±658 | 14.0(7~21) | 84.3±20.1 |
| 1.0 | 6 | 8,690±2,170 | 14.0(10~21) | 481±131 |
| 3.0 | 6 | 27,400±7,880 | 14.0(14~42) | 1,790±650 |
mean±SD
a)中央値(最小値~最大値)
注)ランマーク®の承認された用量は120mgである*。
*ランマーク®の用法及び用量は以下のとおりである。
〈多発性骨髄腫による骨病変及び固形癌骨転移による骨病変〉通常、成人にはデノスマブ(遺伝子組換え)として120mgを4週間に1回、皮下投与する。
〈骨巨細胞腫〉通常、デノスマブ(遺伝子組換え)として120mgを第1日、第8日、第15日、第29日、その後は4週間に1回、皮下投与する。
(2)反復投与
1)50歳以上の外国人骨粗鬆症患者への反復投与時の薬物動態(AVT03-GL-C01試験)5)(外国人データ)
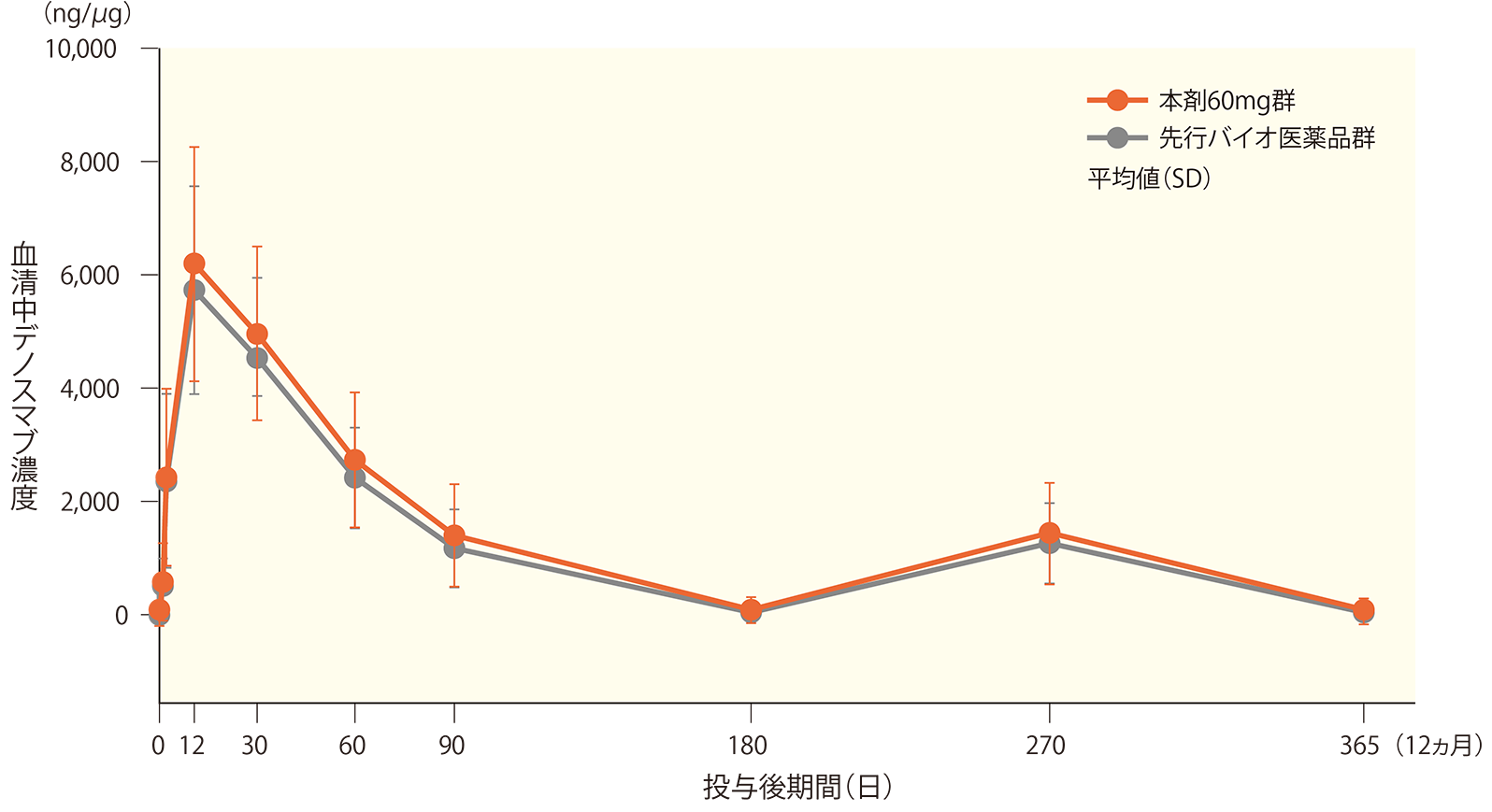
海外において、50歳以上の閉経後骨粗鬆症患者(女性)530例に、本剤60mg又は先行バイオ医薬品(US)の60mg製剤*を初回及び6ヵ月目に皮下投与したときの血清中濃度の推移を以下に示す。
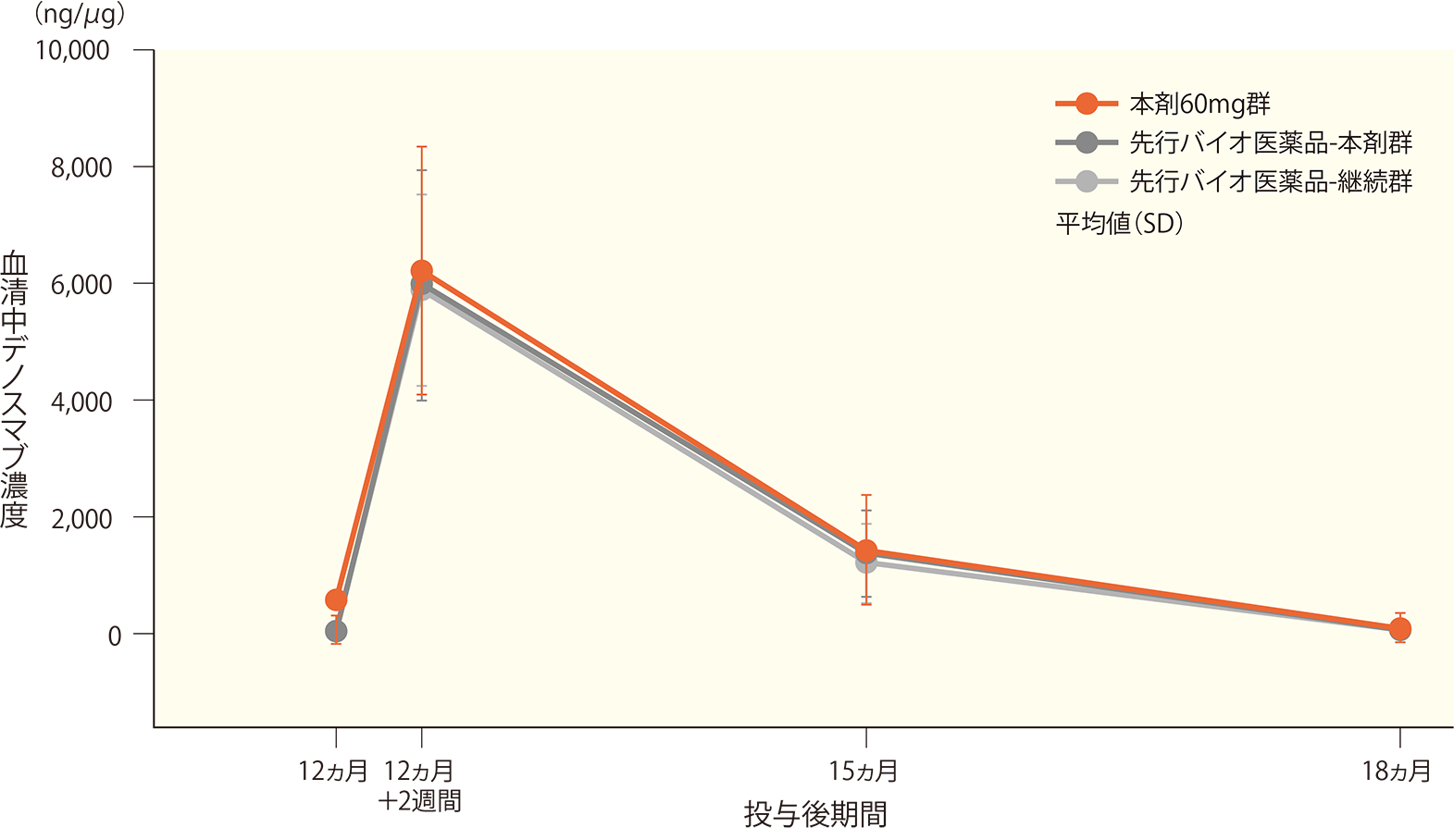
同様に、本剤60mgを初回、6及び12ヵ月目に皮下投与(本剤60mg群)、先行バイオ医薬品(US)の60mg製剤を初回及び6ヵ月目に皮下投与、本剤60mgを12ヵ月目に皮下投与(先行バイオ医薬品-本剤群)、先行バイオ医薬品(US)の60mg製剤を初回、6及び12ヵ月目に皮下投与(先行バイオ医薬品-継続群)したときの血清中濃度の推移も以下に示す。
*先行バイオ医薬品(US)の60mg製剤は米国で承認されているプラリア®〔デノスマブ(遺伝子組換え)製剤〕を指す。
| ベース ライン | 1日 | 2日 | 12日 | 30日 | 60日 | 90日 | 180日 | 270日 | 12ヵ月 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 本剤 60mg群 | 11.090 (176.6331) (n=264) | 579.313 (689.5045) (n=265) | 2425.295 (1580.2112) (n=264) | 6197.599 (2088.3154) (n=253) | 4960.095 (1541.9528) (n=259) | 2722.731 (1203.3533) (n=258) | 1404.333 (904.2722) (n=262) | 83.153 (228.1823) (n=253) | 1438.491 (905.3787) (n=245) | 88.173 (239.8484) (n=242) |
| 先行バイオ 医薬品群 | 0.020 (0.3274) (n=266) | 516.544 (495.1832) (n=265) | 2366.898 (1549.5230) (n=265) | 5739.008 (1856.8706) (n=262) | 4548.785 (1411.7180) (n=260) | 2433.281 (891.0038) (n=256) | 1175.485 (690.4215) (n=258) | 46.288 (131.5979) (n=251) | 1271.502 (710.2819) (n=246) | 40.645 (89.6341) (n=244) |
血清中デノスマブ濃度(ng/μg)、平均値(SD)
【デノスマブBS皮下注120mgRM「F」の組成・性状、効能又は効果、用法及び用量】
3. 組成・性状(抜粋)3.1 組成 販売名:デノスマブBS皮下注120mgRM「F」、有効成分:1バイアル(1.7mL)中デノスマブ(遺伝子組換え)注)[デノスマブ後続1]120mg、添加剤:1バイアル(1.7mL)中L-ヒスチジン 0.524mg、L-ヒスチジン塩酸塩水和物 1.07mg、精製白糖 140mg、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 0.51mg
注)本剤は遺伝子組換え技術によりチャイニーズハムスター卵巣(CHO)細胞を用いて製造される。
4. 効能又は効果
多発性骨髄腫による骨病変及び固形癌骨転移による骨病変
6. 用法及び用量
通常、成人にはデノスマブ(遺伝子組換え)[デノスマブ後続1]として120mgを4週間に1回、皮下投与する。
| 12ヵ月 | 12ヵ月+2週間 | 15ヵ月 | 18ヵ月 | |
|---|---|---|---|---|
| 本剤60mg群 | 88.173 (239.8484) (n=242) | 6225.159 (2125.5839) (n=242) | 1445.141 (946.8337) (n=241) | 109.141 (256.1045) (n=237) |
| 先行バイオ医薬品-本剤群 | 44.444 (91.5902) (n=122) | 5974.953 (1973.2968) (n=120) | 1377.690 (740.1135) (n=121) | 75.353 (141.9690) (n=119) |
| 先行バイオ医薬品-継続群 | 36.846 (87.8469) (n=122) | 5875.246 (1653.3838) (n=122) | 1210.361 (682.1949) (n=121) | 47.399 (105.0398) (n=118) |
血清中デノスマブ濃度(ng/μg)、平均値(SD)
2.吸収(日本人及び外国人データ)
※デノスマブBS皮下注120mgRM「F」電子添文より
健康な成人、低骨密度又は骨粗鬆症の閉経後女性及びがん患者に本剤を皮下投与したときの絶対バイオアベイラビリティは約62%であった6)(日本人及び外国人データ)注)。
注) 母集団薬物動態解析による推定値
3.分布(サル)
サルに125I標識した本剤1mg/kgを単回皮下投与したとき、組織中の放射活性は、投与部位と腋窩リンパ節を除き、血清中より低かった。血清に次いで鼠径リンパ節、脾臓、卵巣及び肺に高い放射活性が認められた7,8)。分布に関する明らかな性差は認められなかった7)。
4.代謝
本剤はヒトIgG2サブクラスに属するモノクローナル抗体であることから、他の免疫グロブリンと同様に生体内での異化により消失すると推察される7,9)。
5.排泄(サル)
サルに125I標識した本剤1mg/kgを単回皮下投与したとき、投与された放射能は投与後56日までに77.9%が尿中に排泄された7)。
6.腎機能障害患者(外国人データ)
腎機能正常者12例及び腎機能障害患者43例(軽度腎疾患13例、中等度腎疾患13例、重度腎疾患9例、透析の必要な末期腎不全患者8例)に本剤60mg注)を単回皮下投与したとき、血清中デノスマブのCmax及びAUCに、腎機能障害の程度による明らかな差異は認められなかった10)(外国人データ)。[17.3.1参照]
注)ランマーク®の承認された用量は120mgである*。
*ランマーク®の用法及び用量は以下のとおりである。
〈多発性骨髄腫による骨病変及び固形癌骨転移による骨病変〉通常、成人にはデノスマブ(遺伝子組換え)として120mgを4週間に1回、皮下投与する。
〈骨巨細胞腫〉通常、デノスマブ(遺伝子組換え)として120mgを第1日、第8日、第15日、第29日、その後は4週間に1回、皮下投与する。
薬効薬理
1.作用機序
※デノスマブBS皮下注120mgRM「F」電子添文より
デノスマブは特異的かつ高い親和性でヒトRANKLに結合するヒト型IgG2モノクローナル抗体である11,12)。
RANKLは膜結合型あるいは可溶型として存在し、骨吸収を司る破骨細胞及びその前駆細胞の表面に発現する受容体であるRANK注)を介して破骨細胞の形成、機能及び生存を調節する必須の蛋白質である13)。
多発性骨髄腫及び骨転移を有する固形癌の骨病変においては、RANKLによって活性化された破骨細胞が骨破壊の主要な因子である14)。デノスマブはRANK/RANKL経路を阻害し、破骨細胞の活性化を抑制することで骨吸収を抑制し15-17)、がんによる骨病変の進展を抑制すると考えられる。
注)RANK:receptor activator for nuclear factor-κB
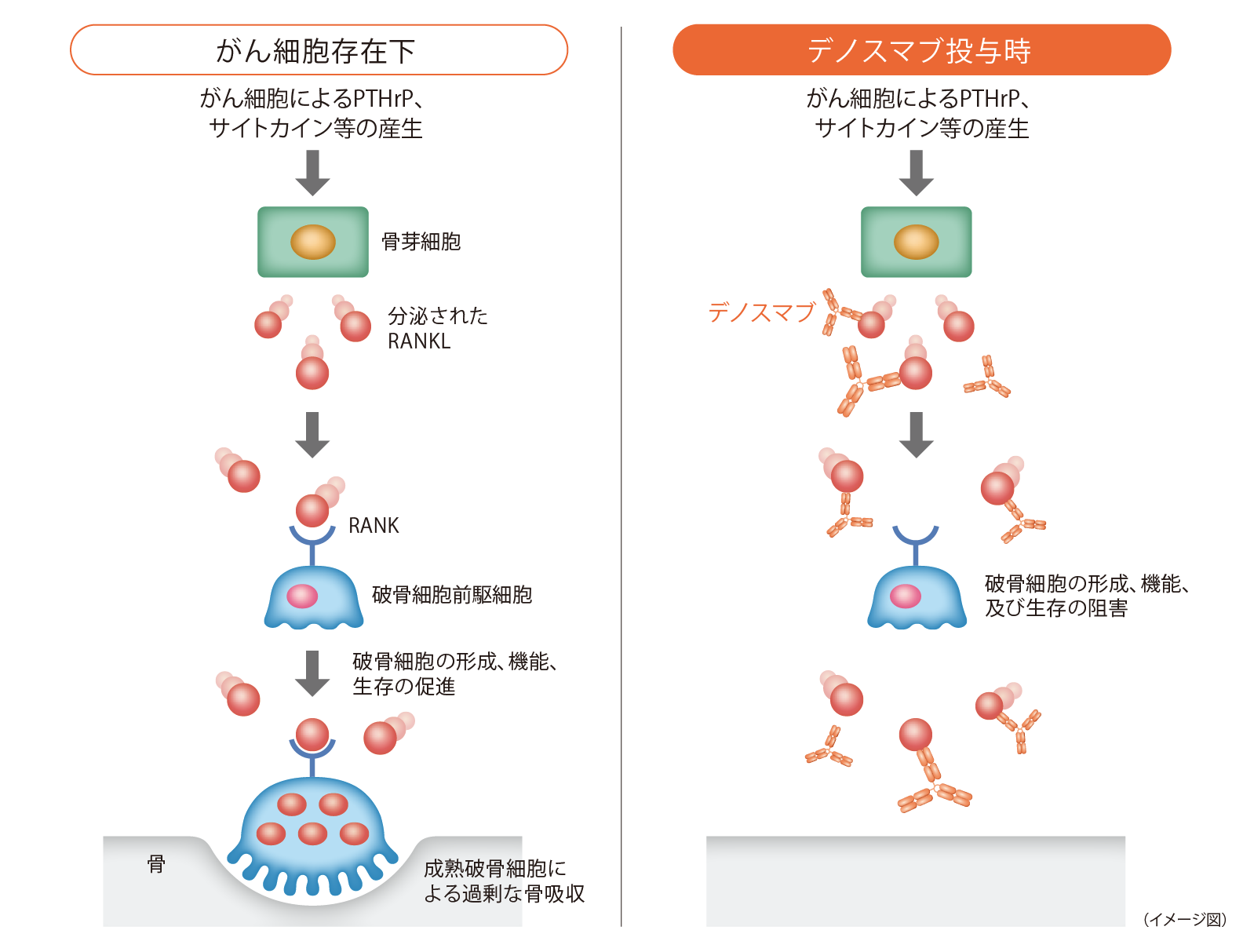
通常、骨内に侵入したがん細胞は副甲状腺ホルモン関連タンパク(PTHrP)及びサイトカイン等を産生し、骨芽細胞等におけるRANKリガンド(RANKL)発現を促進させる。破骨細胞前駆細胞及び破骨細胞の細胞表面に発現している受容体RANKにRANKLが結合することによって活性化し、破骨細胞の形成、機能及び生存が促進され、過剰な骨吸収が引き起こされると考えられる14)。
一方で、デノスマブはRANKLを阻害する。RANK/RANKL経路が阻害されることで、破骨細胞の活性化が抑制され、骨吸収が抑制される16)。その結果、がんによる骨病変の進展を抑制すると考えられる。
デノスマブの作用機序
24, 26)より作図
2.非臨床試験
(1)RANKL結合作用18)
1)RANKL結合作用(in vitro)
本剤、先行バイオ医薬品(EU)*1及び先行バイオ医薬品(US)*2のRANKLへの結合作用を表面プラズモン共鳴法で評価したときの結果は以下のとおりであった。
| 相対RANKL結合親和性 (標準品に対する活性比) | |
|---|---|
| 本剤 (n=7) | 95.8~104.6% |
| 先行バイオ医薬品(EU) (n=21) | 86.0~107.5% |
| 先行バイオ医薬品(US) (n=21) | 80.0~111.2% |
*1 先行バイオ医薬品(EU)は欧州で承認されているプラリア®、ランマーク®〔ともにデノスマブ(遺伝子組換え)製剤〕を指す。
*2 先行バイオ医薬品(US)は米国で承認されているプラリア®、ランマーク®〔ともにデノスマブ(遺伝子組換え)製剤〕を指す。
2)RANK活性阻害作用(in vitro)
本剤、先行バイオ医薬品(EU)*1及び先行バイオ医薬品(US)*2のRANKL誘導性RANK活性阻害作用を、ヒト骨肉腫細胞株(Saos-2)にRANKを発現させた細胞を用いて評価したときの結果は以下のとおりであった。
| 相対RANKL誘導性RANK活性阻害作用 (標準品に対する活性比) | |
|---|---|
| 本剤 (n=7) | 95~102% |
| 先行バイオ医薬品(EU) (n=21) | 96~109% |
| 先行バイオ医薬品(US) (n=21) | 95~110% |
*1 先行バイオ医薬品(EU)は欧州で承認されているプラリア®、ランマーク®〔ともにデノスマブ(遺伝子組換え)製剤〕を指す。
*2 先行バイオ医薬品(US)は米国で承認されているプラリア®、ランマーク®〔ともにデノスマブ(遺伝子組換え)製剤〕を指す。
(2)骨吸収抑制(サル)
※デノスマブBS皮下注120mgRM「F」電子添文より
カニクイザルにデノスマブを月1回反復皮下投与すると、投与期間中、尿中I型コラーゲン架橋N-テロペプチドの低下が持続した19)。
(3)骨病変の進展抑制(マウス)
デノスマブはマウスのRANKLに結合しないため、マウス骨転移モデルではマウスのRANKLに結合して阻害するOPG-Fc注)をデノスマブの代替15,16)として使用した。乳癌20-22)(溶骨性又は溶骨性と造骨性の混合型)、前立腺癌23)及び非小細胞肺癌24)(いずれも溶骨性)のマウス骨転移モデルにOPG-Fcを投与したところ、がんによる骨病変の進展が抑制された。
注)OPG-Fc:免疫グロブリン結晶化フラグメントに結合させたオステオプロテゲリン
安全性薬理試験及び毒性試験
日本、欧州及び米国のバイオ後続品の開発に関して適用される規制ガイドラインに従い、安全性薬理試験及び毒性試験は実施していない。
- 社内資料:国内第Ⅰ相臨床試験成績(AVT03-GL-P03)[承認時評価資料]
- Yonemori K, et al.: Cancer Sci. 2008; 99(6): 1237-1242
- Kumagai Y, et al.: Bone. 2011; 49(5): 1101-1107
- 試験20030164(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.7.2.2.1.3)
- 社内資料:海外第Ⅲ相臨床試験成績(AVT03-GL-C01)[承認時評価資料]
- 薬物動態解析(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.7.2.3.7.1)
- 薬物動態試験の概要文(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.6.4)
- 分布(ランマーク皮下注120mg:2012年1月18日承認、審査報告書)
- 代謝(ランマーク皮下注120mg:2012年1月18日承認、審査報告書)
- Block GA, et al.: J Bone Miner Res. 2012; 27(7): 1471-1479
- 薬理試験(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要3.2.1)
- 起原又は発見の経緯(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要1.5.2)
- Lacey DL, et al.: Cell. 1998; 93(2): 165-176
- Roodman GD, et al.: Cancer Treat Rev. 2008; 34(1): 92-101
- 効力を裏付ける試験(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.6.2.2)
- Kostenuik PJ, et al.: J Bone Miner Res. 2009; 24(2): 182-195
- 老齢huRANKLノックインマウスにおけるデノスマブの薬理試験(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.6.2.2.2.3)
- 社内資料:薬理作用に関連する試験 -RANKLに対する結合活性-[承認時評価資料]
- 若齢無去勢カニクイザルを用いた12カ月投与による薬理学的パラメータ(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.6.2.2.2.4)
- 乳癌骨転移マウスモデルにおけるRANKL阻害(OPG-Fcによる)の薬理(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.6.2.2.3.2)
- Morony S, et al.: Cancer Res. 2001; 61(11): 4432-4436
- Canon JR, et al.: Clin Exp Metastasis. 2008; 25(2): 119-129
- PC-3異種移植マウスモデルにおける前立腺癌骨転移の進行に対するOPG-Fc単独及びドセタキセルとの併用によるRANKL阻害の薬理(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.6.2.2.3.3)
- 肺癌骨転移マウスモデルにおけるRANKL阻害(OPG-Fcによる)の薬理(ランマーク皮下注120mg:2012年1月18日承認、申請資料概要2.6.2.2.3.4)


